ホーム > プレスリリース > 2012年 > 5月9日発表
調査レポート発刊のお知らせ
世界のバイオシミラー(*)開発の現状と将来展望
〜開発競争とともに提携競争もすでに始まっている〜
[本書のポイント]
• 国内外ですでに始まっている開発競争。先行しているのは欧州。
• 自社単独での参入は難しい。
• バイオシミラーは先行バイオ医薬品の牙城を崩せるのか?
(*)バイオシミラー : 特許切れバイオ医薬品の後発薬。ただし、先発品と同一成分でなくとも可。
市場調査・コンサルティング会社の株式会社シード・プランニング(本社:東京都文京区 梅田佳夫社長、以下シード・プランニング)は、このほど、「世界のバイオシミラー開発の現状と将来展望」を発刊いたしましたのでお知らせします。
現在、巨大な市場を築いているバイオ医薬品は、数年以内に特許失効を迎えます。また、近年、画期的な新薬のシーズ探索が難しくなっており、各医薬品メーカーは岐路に立たされています。そのような状況の中、バイオ医薬品の後発薬(バイオシミラー、バイオ後続品、フォロー・オン・バイオロジックスともいう)に新たな活路を見出す企業が増え始めました。しかし、バイオ医薬品は製造、開発に膨大なコストがかかります。さらに、規制当局にも、後発品の承認方法を明確に決められないという事情があります。
本レポートは、バイオシミラーの製造・開発側、および、規制側双方の課題を明らかにしながら、バイオシミラー市場を展望したものです。
本書のポイントと概要は以下の通りです。
本書のポイント
◆ 国内外ですでに始まっている開発競争。先行しているのは欧州。
• 欧州が先行している。日本では2製品が承認済み。
• 米国では未だ正式にバイオシミラーとして承認していない。
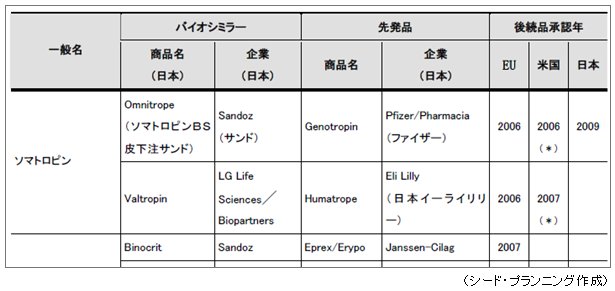
バイオシミラーで先行しているのは欧州。2006年、世界初のバイオシミラー「Omnitrope」がノバルティスの子会社であるサンドから発売された。先行バイオ医薬品(参照医薬品)はファイザーの遺伝子組み換えヒト成長ホルモン製剤・ソマトロピン(商品名:Genotropin)である。
その後、腎性貧血治療薬エポエチン(エリスロポエチン)、および顆粒球コロニー刺激因子(G-CSF)・フィルグラスチムのバイオシミラーも数種類発売された。
国内初承認のバイシミラーは、2009年6月に承認されたサンドの「ソマトロピンBS皮下注『サンド』」(海外では「Omnitrope」)である。2009年3月、厚生労働省より「バイオ後続品の品質・安全性・有効性確保のための指針」が公表されたことに基づき、バイオ後続品として審査された。先行バイオ医薬品であるファイザーの「ジェノトロピン」の7割の薬価となった。
国内企業が始めて開発したバイオシミラーは、2010年5月に発売された日本ケミカルリサーチ(JCR)とキッセイ薬品の共同開発による「エポエチンアルファBS注『JCR』」。先行バイオ医薬品は協和発酵キリンの「エスポー」である。薬価は先行バイオ薬品の77%の価格と決まった。これは2010年4月より施行された新薬価制度に基づき算定された。
米国では先発品メーカーと後発品メーカーの攻防が激しく、FDAはバイオシミラーを未だ正式に承認していない。例外的に2製品承認されているが、FDAはあくまで新薬として承認したものである。
なお、本書には日米欧で承認されている主なバイオシミラー(2012年1月現在)の一覧を収録している。
<以下、本書の一部を抜粋>
◆ 自社単独での参入は難しい。
◆ バイオシミラーは先行バイオ医薬品の牙城を崩せるのか?
• 市場はまだ小さい。世界市場は2015年に20億米ドルに(シード・プランニング予測)。
• 日本市場は2016年でも50億円未満(シード・プランニング予測)。
• よって他社との提携により、グローバルな販売網を構築すべき。
バイオシミラーの市場はまだ小さい。2010年の世界の市場規模は3億米ドル程度と推定される。ヒト成長ホルモン、エリスロポエチン、G-CSFの3製剤の世界市場に占めるバイオシミラーの割合は2%未満である。主要各国でのバイオシミラーの薬価は先行バイオ医薬品の70〜90%程度であるため、現在の上市品に限れば先発品とバイオシミラーの薬価差は大きくない。また、世界最大の医薬品市場である米国でバイオシミラーが本格的に普及していない。
現在開発中の抗体医薬品のバイオシミラーが2015年以降に普及し始め、世界市場は20億米ドルに拡大すると予想される。
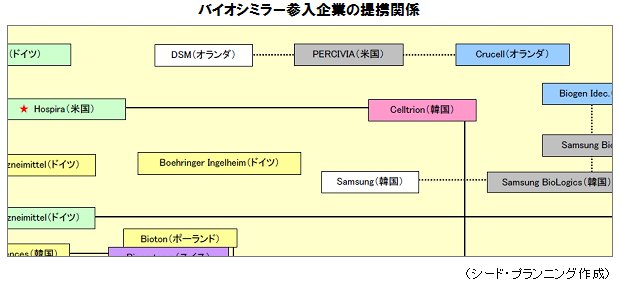
バイオ医薬品製造のハードルを越え、市場を開拓するには1社単独では難しいため、各社の提携競争がすでに始まっている。
本書の概要
- レポート名
- 世界のバイオシミラー開発の現状と将来展望
- 発刊日
- 2012年4月25日
- 体裁
- A4 /183ページ
- 販売価格
- 180,000円+消費税
- 発行
- 株式会社シード・プランニング
- 掲載項目
-
バイオシミラー参入企業の提携関係図
開発中の主なバイオシミラー
Ⅰ 総括
1 バイオシミラーの最新動向
2 バイオシミラーの市場展望
Ⅱ バイオシミラーの最新動向と将来展望
1 バイオシミラーが求められる背景
2 バイオシミラーに関する規制
3 世界のバイオシミラー市場
4 バイオシミラー周辺ビジネス
Ⅲ バイオ後続品の品質・安全性・有効性確保のための指針
Ⅳ 企業個票 (39社)
1 あすか製薬
2 協和キリン富士フイルムバイオロジクス
3 ジーンテクノサイエンス
4 日医工
5 日本化薬
6 日本ケミカルリサーチ
7 ニプロ
8 富士製薬工業
9 Meiji Seika ファルマ
10 持田製薬
11 Actavis Group PTC ehf
12 Amgen Inc
13 Aprogen Inc
14 Baxter International Inc
15 Biogen Idec, Inc
16 Biopartners GmbH
17 BioXpress Therapeutics SA
18 Boehringer Ingelheim GmbH
19 Celltrion, Inc
20 Dong-A Pharm. Co., Ltd.(東亞製薬)
21 Dr. Reddy' s Laboratories Ltd
22 Gedeon Richter Plc
23 GH Genhelix, S.A
24 Hanmi Pharmaceutical Co. Ltd
25 Hanwha Chemical Corp
26 Hospira, Inc
27 LG Life Sciences
28 Medice Arzneimittel Pütter GmbH & Co.KG
29 Merck & Co., Inc
30 Mylan Inc
31 Pfizer Inc
32 Ranbaxy Laboratories Ltd
33 Royal DSM N.V
34 Samsung Biologics
35 Sandoz International GmbH
36 Spectrum Pharmaceuticals
37 STADA Arzneimittel AG
38 Teva Pharmaceutical Industries Ltd
39 Viropro, Inc
〒113-0034
東京都文京区湯島3-19-11 湯島ファーストビル 4F
TEL : 03-3835-9211(代) / FAX : 03-3831-0495
E-mail : info@seedplanning.co.jp
担当 : 渡部(わたべ)・野田(のだ)